

研究の目的: この試験の主たる目的は、WOMAC スコ ア、6分間の無痛歩行距離(MWD)およびレスキュー 鎮痛薬の必要性を検討することによって、天然ミネラル濃縮溶液(Natural Mineral Concentrate Solution)が軟 骨保護剤として作用するかどうかを判断することである。
方法論: 膝関節の中程度の変形性関節症を有する100人 の患者における二重盲検プラセボ対照無作為試験を実 施した。 天然のミネラルサプリメント(NMCS)40 滴を試験群に1日1回投与した。 関節軟骨の厚さ、関節 隙幅(JSW)および滑液組成の変化を評価することにより、有効性を客観的に確認した。
結果: 24週間の観察により、プラセボ群と比較して 、WOMACスコアおよびNMCS群の6 MWD(6分間の無 痛歩行距離)の有意な差が認められた。 超音波検査お よび滑液検査により、軟骨構造の改善が明らかになっ た。 (被験者は)治療を十分に許容でき、また、群間に おいて有害事象のプロファイルに有意な差は認められ なかった。
序論
ミネラルは身体機能の多くにとって重要であり、細胞 内部のミネラル組成が、わずかに損なわれただけでも 、深刻な生理学的影響を及ぼす可能性がある(8)。
亜鉛、銅、セレン、マグネシウムおよびマンガンのような鉱物および、ビタミンA、EおよびC、ナイアシン 、パントテン酸、オメガ3脂肪酸、コンドロイチン、 グルコサミン、コラーゲン、ヒアルロン酸、およびヒ アルロン酸を含むホウ素、黄含有アミノ酸のような微 量元素は、硫軟骨基質の産生において重要な役割を果 たすこと示唆されている(6,23)。
マグネシウム、銅、マンガン、セレン、亜鉛などの天 然鉱物は、動物実験とヒト研究の両方で抗炎症効果を 示す。 変形性関節症のラットを使用した試験では、食 物マグネシウムの欠乏が軟骨損傷の度合いを増加させ ることが示された(12)。 さらに、食事中のマグネシウムの増加は、炎症誘発性プロテインC反応性タンパ ク質の血清レベルを低下させることによって炎症に影 響を及ぼす可能性がある(22)。
微量元素である銅は 、コラーゲン架橋剤リシルオキシダーゼのような酵素 の必須補因子である。
最近の資料によると、関節の抗酸化状態の不均衡から 生じる活性酸素種の過剰は、軟骨の劣化および関節の 変形を引き起こす可能性がある(9)。
抗酸化酵素ス ーパーオキシドジスムターゼは補因子として銅、亜鉛 およびマンガンを必要とする。Haqqi によるヒト軟骨 外植片モデルでは、ミネラル補給がIL-1βに応答して軟 骨分解を減少させ、また誘導性一酸化窒素シンターゼ の誘導による二次的な酸化窒素生成を示した (4,18)。
グルタチオンペルオキシダーゼの必須補因子であるセレンも、骨関節炎病変の発生率を低下させる役割を担 っている[13,21]。
ホウ素、マンガンおよびセレンは、 病因を遅くし、したがって変形性関節症の病変の出現 および変形性関節症における症状の重症度を低下させ ることが報告されている(6)。
海草由来のマルチミネラルサプリメント (Aquamin)、シエラ山脈の鉱物由来製品 (Sierrail)、および Phytalgic に関する研究では、12 週間の治療により、WOMACの疼痛、活動、複合体お よび硬さのスコア、ならびに6MWDおよびNSAIDの使 用量の部分的な低減がみられた (5,10,11,19)。
グルコサミンおよびコンドロイチン単独での有効性に 関する研究では、効果についてばらつきのある結果が 生じ、このアプローチには一定の制限がある可能性が あることが示唆される。補因子、特にミネラルや微量 元素の摂取が不適切であることが原因である可能性が 考えられる(16)。
関節痛を有する患者に対してミネラルが有益な効果を 示した以前の研究に基づいて、治療上の効果を主張す ることなく、膝の変形性関節症において有益な効果の 有無を主観的かつ客観的に評価した。
この臨床試験の対象である食品サプリメントは、ユタ 州のグレートソルト湖の成分から濃縮された、72種以上のイオン形態の天然ミネラルを含む濃縮微量ミネラ ルドロップ(NMCS)である。 他の成分を加えずに 100%天然である。 NMCSの典型的なミネラル組成に ついては、Table 1を参照のこと。
選択基準は、NSAIDまたは鎮痛剤の使用によらず、膝 に症候性原発性変形性関節症を呈し(1)、50歳以上、週 1回以上の鎮痛剤もしくはWOMACの使用にかかわらず 過去3ヶ月間の毎日の疼痛があり、病歴としての朝の 硬直が30分未満であり、対象となる膝における WOMACスコアが≦75であることと定義する。
X線撮影の基準には、Kellgren Lawrence による膝関節 変形性関節症のグレードスケール 0、1、2 または 3(Table 2)、Brandtによる骨関節炎のX線撮影グレー ドスケール 1および2(Table 3)、および Ahlback に よる脛骨大腿関節の変形性関節症のX線撮影グレード スケール 0 および 1(Table 4)を適用した。 両方の膝 が症状を呈した場合、より痛い方だけを考慮した。
主な除外基準は、二次膝変形性関節症、重症変形性関 節症(JSW <2 mm)、3ヵ月以内の前関節内注射およ びコルチコステロイドがある者、3カ月以内にジアセ リンによる治療歴のある者、および臨床的に重要な全 身性疾患患者とした。

Table 1. NMCS のミネラル組成

Table 2. Kellgrenのグレードスケール

Table 3. Brandt による 放射線写真における脛骨大腿関節の変形性関節症のグレードスケール

Table 4. Ahlback による放射線写真における脛骨大腿関節の変形性関節症のグレードスケール
二重盲検法により合計 100 人の被験者を濃縮ミネラ ルドロップ治療群またはプラセボ群のいずれかに登録 し、 NMCSおよびプラセボをそれぞれ24週間投与した。
被験者は空腹時に6ヶ月間NMCSを1日2回服用することを勧められた。 1週間に1日5〜10滴から40滴(1/2 ティースプーン(tsp))まで用量を徐々に増加させた。
開始時点の訪問に際し、被験者のバイタルサインを検 査するとともに各種検査を実施した。 具体的には 、WOMACスコア、6MWD、関節スペース幅、関節軟 骨の厚さおよび滑液の細胞性について測定を行った。 最初の1ヶ月間は週に1度、被験者に対して有害事象 および救急医療(NSAIDS)の必要性についての評価 をおこなった。 その後は、6ヶ月経過時点まで毎月フ ォローアップを行った。
WOMACスコアと6 MWDについては毎月評価を行っ た。X線、超音波検査、滑液検査、およびその他の検 査は、6ヶ月の期間終了時点でのみ再度測定を行った。
ウェスタンオンタリオおよびマクマスター大学の関節 炎指数(WOMAC)(2,14)は、痛みのある関節の可動性および身体障がいの程度について患者の主観評価 方法として広く使用されている尺度である。 疼痛、 剛性および身体機能の3つの観点から評価を行いそれ ぞれ5問、2問、17問の質問で評価を行う。 最大スコ アは合計で 96点、最小は0点となる。各観点の得点ス ケールは、それぞれ最大20点、8点、68点となる。 Andrea Mankoskiによって設計された痛みスケール (Table 5参照)は、重症度を非常に正確に表してお りこれも使用した。
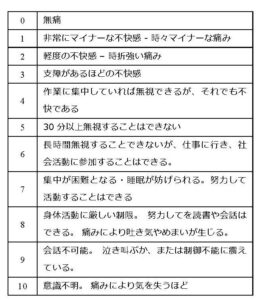
Table 5. Andrea Mankoskiによる痛みスケール
6分の歩行距離では、屋内の廊下に50メートルの距離 をマーキングしたうえで、被験者に6分以上できるだ け早く歩くように伝え歩行距離を測定・記録した。 (15)
以前に公表されたガイドラインに沿い、X線源から1 メートルのところに立つ体重保持姿勢で関節を完全に 伸ばした患者の、膝関節の前後のX線写真を撮影した 。幅は、JSW(最小JSW)の最も狭い点を測定した 。 以前に報告に基づき、基準は JSN> 0.50mm と定 義した(15)。
超音波検査では、体重を支える顆の関節軟骨は、鋭い 前縁および後縁を有する低エコーの帯として現れる。 顆間領域(8-10mm)が最も厚く、大腿骨顆上が最も 薄い(平均4~5mm)(3,24)。
耐容性および安全性評価には、患者が示した症状およ び徴候、ならびに実験室ベースの血液学的および生化学的アッセイに基づいて行った。副作用は、被験者の 日常活動への干渉程度(軽度・中程度・重度)に基づ いて、単離、断続または連続として分類した。また 、NMCSとの因果関係の可能性については、確定的/ ありうる/おそらく/判定不能 と区分して判定を行った 。 研究内容は倫理委員会によって承認され、また、 すべての患者は内容について十分に周知されたうえで 、研究への参加について書面による同意をおこなった 。
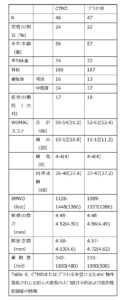
Table 6 は、4つのグループすべてが対象数、性別、 体重、年齢、WOMACスコア、6MWD、平均関節スペ ース幅、平均関節軟骨の厚さおよび細胞数において比 較可能であり、これらの項目においてランダム化が有効であったことを示している。
NMCS患者4名およびプラセボ群3名は試験を完了し なかった。 中止の理由は、個人的なものまたは試験 が無効となったためである。
このうちNMCS群の患者 の1人は吐き気を訴えたが、中断後は正常に戻った。 両群とも、24週間の治療期間をとおし、WOMAC値 の基準値からの改善を示した(Table 7)。 改善の程 度は、NMCS群で有意に大きかった(p <0.005)。 4 週間、8週間、12週間の治療時点においては、NMCS 群はベースラインに対して顕著な改善を示したが、プ ラセボと比較して有意ではなかった(p> 0.05)。
試験群の複合体WOMACスコアは、12週および24週 それぞれにおいてプラセボ群が4.3および7.1であるの と比較して、NMCS 群では 7.1および16.2と有意に改 善した。12 週時点で、5点スコアが低下したと報告を した数は、プラセボ群で4人(8%)であったのに対 し、NMCS 群では16人(34 %) であった。24週間経過 時点では、プラセボ 21%(n = 10)に対して NMCS 52%(n = 24)とさらに改善した。
12週時点、24週時点における疼痛、剛性および活動 性スコアにおいて、NMCS 群では、それぞれ 1.5点 、0.6点、5点 から 4点、1.2点、11点に改善されたの に対し、プラセボ群では、1点、3点、3点 から 1.8点 、0.4点、5点 と有意な変化が認められなかった。
痛み、剛性および活動スコアについては、12週時点 でNMCS群では、それぞれ 15人、4人、20人の患者 において少なくとも1ポイント減少したのに対し、プ ラセボ群では それぞれ 5人、2人、6人といういう結 果であった。さらに、24週時点では、NMCS群 28人 、10人、30人(60%、21%、65%)であったのに対 し、プラセボ群 10人、4人、18人 (21%、8%、38%)であった。
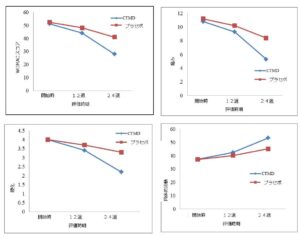
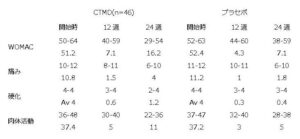
6分間に無痛状態で歩行可能な距離は、NMCS 群内で は時間の経過と共に 80フィートおよび 122フィート と有意に改善された。 プラセボ群でも、30フィートおよび 46フィートと改善が認められたが有意ではな かった。100 フィートの改善を示した人数は、12週 時点、24週時点で、NMCS 群では、それぞれ 12人(26%)および15人(32%)であったのに対し、プ ラセボ群では5人(10%)および8人(17%)であっ た。NMCS群18人およびプラセボ群30人に対して、 週に少なくとも1回(パラセタモールを1日4回500mg に制限した投与)レスキュー投薬が必要であった。 さらに、プラセボ群と比較して、NMCS群ではパラセ タモールの使用が23%減少した。
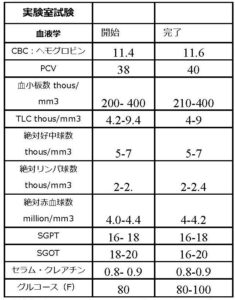
Table 8:
X線検査では有意な変化を認めることができなかった。 いずれの群においてもJSWの増加は認められなかった。関節スペースの幅が少なくとも0.01 mm減少したケースは、NMCSが4人(8%)であったのに対し、プラセボでは10人(21%)と、NMCS群のほうが良好な結果であった。
軟骨の厚さを測る超音波検査では、NMCS群では、6人(13%)において少なくとも0.01 mm増加し、4人(8%)が少なくとも0.01 mmの厚さを失っていた。 プラセボでは、2人(4%)のみが厚さが増加したが、10人(21%)は少なくとも0.01mm厚さを失っていた。
滑液検査では、NMCSが滑液流動性および滑液代謝の回復および軟骨病変の軽減に役立つことを示唆された。 細胞数が500未満の被験者数は、NMCS群では治療前10人(21%)、24 週時点では 25人(54%)であった。 プラセボでは、治療前の11人(23%)、24 週時点では 16人(34%)であった。NMCS群では細胞数の平均が240、プラセボでは430に減少した。
有害事象は、試験群では14例、対照群では10例とやや均等な分布であった。 4人(8%)の患者において、有害事象はミネラルの摂取に関連する可能性があると考えられた。 被験者の1人は耐性が低いとの理由で試験を中止した。 有害事象は上部消化管不快感に関連したものであったが、両方のグループで8週間までに完全に解消した。 Table 8にある血液学的および生化学的安全変数の要約はNMCSは絶対的に安全であることを示している。
本試験の結論に至るまでの5つの中間評価点において、血圧、呼吸数および脈拍数の有意な変化は認められなかった。NMCS群の4人の患者においてのみ、最初の1週間で脈拍数がスクリーニング値76.2±1.2から81.4±1.5まで増加した。 同様に、試験群においてのみ、最初の1週間に、6人の患者で一過性の上昇血圧が認められた。
COX-2阻害剤による心臓血管疾患および脳卒中のリスク増加、非選択的COX阻害剤に関連した重要な胃腸障害、腎臓合併症および早期死亡などに関する最近の文献、ならびにNSAIDクラスは、発病を抑制するのではなく、症状の緩和を提供するものであるという点を考慮すると、代替案の必要性が非常に高い。
天然ミネラルサプリメントNMCSは、市場での入手が容易で、天然源からの派生物であり、すでに一般消費者によって使用されているために選択された。これらのミネラルは、相互作用する他の元素とのバランスが取れていると最も効果的を発揮する。 1つの要素が多すぎると、他の要素に不均衡が生じる可能性があるため、バランスがとれていてイオン的な形の天然由来であることが重要となる。キレート化された形態で結合された微量元素は、身体により容易に利用可能であり、吸収の間に相互作用し相互干渉する可能性は低い。
ミネラルサプリメントの用量は、各種ミネラルの毎日の摂取許容量に関する文献に基づいて決定された。 (8)重篤な変形性関節症を有する患者は、軟骨に重度の損傷があるため除外した。これらの患者の健常な滑膜細胞の数は乏しく、健康な細胞が十分に作用しないため、食事および粘液補充を含む保存的治療からでは最終的に十分な効果を得られないことを意味する。
NMCS治療患者全員において、プラセボと比較して明らかな有益性の発現が有意に早かった。第6週以降には群間の試験差異の結論が有意であることが明白となった。
24週間で歩行距離がNMCS群では 9.6%およびプラセボ群で 3.5%改善した。これらの距離は小さく見えるが、被験者達にとってより重要なのは歩行能力の向上である。
プラセボ群では、疼痛、活動および複合スコアの治療において時間の経過とともに改善が示されたが有意ではなく、示された改善はおそらく以下の理由によるものであった。習慣が健康的に改善に寄与するため、プラセボ群においても第1次および第2次評価の改善を示した。また、試験における治療が全て利益をもたらすと期待していたので、プラセボの応答をもたらした可能性がある。さらに、ミネラルサプリメントの摂取は被験者の基本的な栄養状態に影響を与えた可能性もある。レスキュー投薬の使用はプラセボ群のほうがNMCS群より多く、これが治療群とプラセボ群間における効果の違いを隠している可能性もある。
広範な文献検索を行うも、関節健康におけるミネラル補給の有益な効果を示す客観的な臨床データを示すいかなる研究も得られなかった。本結果を他の二重盲検プラセボ対照試験(5,10,11,19)の主観的データと比較し、それらが同等であると判断した。
比較を行った主な研究データは次のとおり。JOM L. Frestedtet al(WOMAC P <0.001、W MWACの改善は3.5%、MWDは3.5%)、Mark JS Miller(WOMAC合計38〜43%でn = 91改善)救急投薬の使用率が28〜23%、Jacquet A(鎮痛薬の使用が有意に少なかった(P <0.001)、群平均差が-10.0(95%CI) :4.9〜-15.1)。骨関節炎における疾患修飾剤として作用する可能性が別個に示されているように、能動腕における疼痛、剛性および機能に関する平均WOMACスコアは有意に異なり(P <0.001)、変形性関節症において効果を示した。
この天然ミネラルサプリメントがこれらの作用と効果を示す仕組みは不明である。本書は栄養に基づくミネラルの作用と効果的な抗関節炎療法との間の明確な関連性を説明するものではない。 NMCSは複数のミネラルで構成されており、その複合体の「有効成分」を決定することは困難である。多くのミネラル、マンガンおよびセレンは、この独特の複合体の有効性に直接および/または間接的に影響を及ぼし得る抗炎症および抗酸化特性を有し得る。
NMCSは、軟骨の損傷の進行を遅くし、サプリメントとしてその有効性を確認できる。6ヶ月の研究を通じさまざまな臨床的および実験的安全性に変化がなかったので、このミネラルサプリメントが安全であることは明らかである。サプリメントは、特にベースライン条件と比較して有効であったが、プラセボからの持続的な解離を決定づけるのは困難でありさらなる研究が必要である。
一部の患者では1週間という早期からこのような効果が発現したことは、IL-1βの誘導によってヒト軟骨分解が保護されることを示す in vitro 研究と矛盾しない。しかしながら、本研究は、軟骨破壊からの保護に治療がどのように関連するかを直接的に評価するものではなく、またこの限られた期間で関節構造に大きな変化が起こるとも考えにくい。 (17)
MRIは、膝のOAに関連した異常の全スペクトルを調査することができる。また、軟組織構造、軟骨および骨病変の評価も可能であり、よりよい手法ではあるが高価である。しかし、関節症の患者の滑膜および関節軟骨の早期変化をとらえるためには、超音波検査法は単純かつ比較的安価な方法である。MRIと超音波検査法を比較する研究によると、変形性関節症の患者の軟骨変化を評価するため手法として 2 者間に有意な相関があった。
従来型のラジオグラムは、関節関与の重篤度を評価するために一般的に使用されている。しかし、変化は遅れて観察される。 初期の疾患では、OA関節の構造変化は、放射線写真の相対的不感受性のために研究することが困難である。
本研究の主な限界は、短い期間(24週間)、治療停止後の残存効果の評価不足、およびサンプルサイズの制限(群あたり50人)であった。 より多くの被験者に対するより長い治療期間を設定した更なる研究は、NMCSの治療効果を検証し、この24週間の研究期間では十分に示されることがなかった治療効果を探究するのに有用でありる。
変形性関節症の管理に対する代替的なアプローチが望ましい場合、単独または他の栄養補助食品と組み合わせた天然ミネラルサプリメントにより関節の健康を改善し、変形性関節症の症状を有意に緩和すことができる。 効果は4週間以内に明らかとなり、また優れた安全性も示された。
参考文献
膝の骨関節炎の医療管理のためのACRガイドライン2000年更新
Bellamy N Buchanan WW et al。 WOMACの検証研究:股関節または膝の変形性関節症の患者における抗リウマチ薬治療に対する臨床的に重要な患者関連転帰を測定するための健康状態測定器。 J Rheumatol。 1988; 15:1833-1840
Chaojeannie:変形性膝関節症の超音波検査:最近の進歩と将来展望。リウマチ学における最新の見解2008,20(5)
Connor JR、Manning PT、Settle SL、Moore WM、Jerome GM、Webber RK、Tjoeng FS、Currie MG。誘導性一酸化窒素シンターゼの選択的阻害によるアジュバント誘発性関節炎の抑制。 Eur J Pharmacol。 1995; 273:15-24 doi:10.1016 / 0014-2999(94)00672-T
Frestedt JL、Kuskowski MA、Zenk JL:膝関節症のための天然海藻由来のミネラルサプリメント(アクアミンF):無作為化プラセボ対照パイロット試験。 Nutr J. 2009 Feb 2; 8:7
Gaby AR。骨関節炎の自然療法。 Altern Med Rev 1999; 4:330-341に記載されている
Graham DJ、Campen D、Hui R、Spence M、Cheetham C、Levy G、Shoor S、Ray WA。シクロオキシゲナーゼ2選択的および非選択的非ステロイド性抗炎症薬で治療した患者における急性心筋梗塞および急性心臓死のリスク:ネスト化症例対照研究。ランセット2005; 365:475-81
ハリソンの内科の原理第14版第1巻と第2ページ489-492 /ページ446-447 /ページ番号1931
ヘロチンY、Kurz B、Aigner T.酸素および軟骨分解における活性酸素種:友人または敵変形性関節症および軟骨/ OARS、変形性関節症研究協会。 2005; 13:643-654 doi:10.1016 / j.joca.2005.04.002
Girodet PO、Pariente A、Forest K、Mallet L、Moore N. Phytalgic、膝または股関節の変形性関節症の患者におけるプラセボ対無作為化二重盲検プラセボ対照臨床試験 Arthritis Res Ther 2009; 11(6):R192。 Epub 2009 12月16日
ジョイ・L・フリーステッド、メラニー・ウォルシュ、マイケル・ア・クスコフスキー、ジョン・L・ゼンク。天然ミネラルサプリメントは、膝の変形性関節症の症状を緩和します:ランダム化された制御パイロット試験Nutr J. 2008; 7:9
12.キングDE、メインAG、第3、ゲーシーウールソンRF。食事中のマグネシウムおよびC反応性タンパク質レベル。アメリカ栄養学会誌。 2005; 24:166-171。 Kurz B、Jost B、Schunke M.食餌性ビタミンおよびセレンは、機械的に誘発された変形性関節症の発症を減少させ、STR / 1Nマウスの膝関節における抗酸化酵素の発現を増加させる。変形性関節症および軟骨/ OARS、変形性関節症研究協会 2002; 10:119-126を参照のこと doi:10.1053 / joca.2001.0489。 Lequesne M.骨関節炎の重症度および疾患活性の指標。関節炎およびリウマチにおけるセミナー1991; 20(補足2):48-54
13. Lequesne M、Brandt K、Bellamy N、Moskowitz R、Menkes C J、Pelletier J P、et al。変形性関節症における遅効性薬物の試験のためのガイドライン。 J Rheumatol Suppl1994; 41:65-71;議論72-3; erratum、2395
14. McAlindon T.なぜグルコサミンの臨床試験は一様に陽性ではないのですか? Rheum Dis Clin North Am。 2003; 29:789-801 doi:10.1016 / S0889-857X(03)00064-4
15.McAlindon TE、Biggee BA。栄養成分と変形性関節症:最近の動向。 Curr Opin Rheumatol。 2005; 17:647-652 doi:10.1097 / 01.bor.0000175461.57749.46
Miller MJS、Ahmed S、Bobrowski P、Haqqi TM。ユニークなミネラルサプリメント(sierrasil(商標))およびネコの爪抽出物、vincaria(登録商標)J Amer Nutr Assocによる軟骨細胞の分解および軟骨細胞活性化の抑制。 2004; 7:32-39
【請求項2】請求項1に記載の骨関節炎の治療剤。【請求項4】請求項1に記載の骨関節炎の治療剤であって、以下の(a)、(b)、(c)ランダム化比較試験[ISRCTN38432711] Journal of inflammation(London、England) 2005年、2:11
Ravaud P、Auleley G R、Chastang C、Rousselin B、Paolozzi L、Amor B、et al。膝関節距离測定:X線撮影法と関節位置の影響に関する実験的研究。 Br J Rheumatol1996; 35:761-6
19.ササキS、岩田H、石黒N、葉渕O、三浦T.ラットの低セレン食、骨および関節軟骨。栄養学(バーバンク、ロサンゼルス郡、カリフォルニア1994; 10:538-543
膝の骨関節炎の医療管理のためのACRガイドライン2000年更新
Bellamy N Buchanan WW et al。 WOMACの検証研究:股関節または膝の変形性関節症の患者における抗リウマチ薬治療に対する臨床的に重要な患者関連転帰を測定するための健康状態測定器。 J Rheumatol。 1988; 15:1833-1840
Chaojeannie:変形性膝関節症の超音波検査:最近の進歩と将来展望。リウマチ学における最新の見解2008,20(5)
Connor JR、Manning PT、Settle SL、Moore WM、Jerome GM、Webber RK、Tjoeng FS、Currie MG。誘導性一酸化窒素シンターゼの選択的阻害によるアジュバント誘発性関節炎の抑制。 Eur J Pharmacol。 1995; 273:15-24 doi:10.1016 / 0014-2999(94)00672-T
Frestedt JL、Kuskowski MA、Zenk JL:膝関節症のための天然海藻由来のミネラルサプリメント(アクアミンF):無作為化プラセボ対照パイロット試験。 Nutr J. 2009 Feb 2; 8:7
Gaby AR。骨関節炎の自然療法。 Altern Med Rev 1999; 4:330-341に記載されている
Graham DJ、Campen D、Hui R、Spence M、Cheetham C、Levy G、Shoor S、Ray WA。シクロオキシゲナーゼ2選択的および非選択的非ステロイド性抗炎症薬で治療した患者における急性心筋梗塞および急性心臓死のリスク:ネスト化症例対照研究。ランセット2005; 365:475-81
ハリソンの内科の原理第14版第1巻と第2ページ489-492 /ページ446-447 /ページ番号1931
ヘロチンY、Kurz B、Aigner T.酸素および軟骨分解における活性酸素種:友人または敵変形性関節症および軟骨/ OARS、変形性関節症研究協会。 2005; 13:643-654 doi:10.1016 / j.joca.2005.04.002
Girodet PO、Pariente A、Forest K、Mallet L、Moore N. Phytalgic、膝または股関節の変形性関節症の患者におけるプラセボ対無作為化二重盲検プラセボ対照臨床試験 Arthritis Res Ther 2009; 11(6):R192。 Epub 2009 12月16日
ジョイ・L・フリーステッド、メラニー・ウォルシュ、マイケル・ア・クスコフスキー、ジョン・L・ゼンク。天然ミネラルサプリメントは、膝の変形性関節症の症状を緩和します:ランダム化された制御パイロット試験Nutr J. 2008; 7:9
12.キングDE、メインAG、第3、ゲーシーウールソンRF。食事中のマグネシウムおよびC反応性タンパク質レベル。アメリカ栄養学会誌。 2005; 24:166-171。 Kurz B、Jost B、Schunke M.食餌性ビタミンおよびセレンは、機械的に誘発された変形性関節症の発症を減少させ、STR / 1Nマウスの膝関節における抗酸化酵素の発現を増加させる。変形性関節症および軟骨/ OARS、変形性関節症研究協会 2002; 10:119-126を参照のこと doi:10.1053 / joca.2001.0489。 Lequesne M.骨関節炎の重症度および疾患活性の指標。関節炎およびリウマチにおけるセミナー1991; 20(補足2):48-54
13. Lequesne M、Brandt K、Bellamy N、Moskowitz R、Menkes C J、Pelletier J P、et al。変形性関節症における遅効性薬物の試験のためのガイドライン。 J Rheumatol Suppl1994; 41:65-71;議論72-3; erratum、2395
14. McAlindon T.なぜグルコサミンの臨床試験は一様に陽性ではないのですか? Rheum Dis Clin North Am。 2003; 29:789-801 doi:10.1016 / S0889-857X(03)00064-4
15.McAlindon TE、Biggee BA。栄養成分と変形性関節症:最近の動向。 Curr Opin Rheumatol。 2005; 17:647-652 doi:10.1097 / 01.bor.0000175461.57749.46
Miller MJS、Ahmed S、Bobrowski P、Haqqi TM。ユニークなミネラルサプリメント(sierrasil(商標))およびネコの爪抽出物、vincaria(登録商標)J Amer Nutr Assocによる軟骨細胞の分解および軟骨細胞活性化の抑制。 2004; 7:32-39
【請求項2】請求項1に記載の骨関節炎の治療剤。【請求項4】請求項1に記載の骨関節炎の治療剤であって、以下の(a)、(b)、(c)ランダム化比較試験[ISRCTN38432711] Journal of inflammation(London、England) 2005年、2:11
Ravaud P、Auleley G R、Chastang C、Rousselin B、Paolozzi L、Amor B、et al。膝関節距离測定:X線撮影法と関節位置の影響に関する実験的研究。 Br J Rheumatol1996; 35:761-6
19.ササキS、岩田H、石黒N、葉渕O、三浦T.ラットの低セレン食、骨および関節軟骨。栄養学(バーバンク、ロサンゼルス郡、カリフォルニア1994; 10:538-543
20. Shakibaei M、Kociok K、Forster C、Vormann J、Gunther T、Stahlmann R、Merker HJ。 ofloxacin処理マウスおよびマグネシウム欠乏未熟ラットの関節軟骨における超微細構造変化の比較評価。毒性病理。 1996; 24:580-587
Stephen Holt。代替療法および相補療法。骨および関節の健康1998年4月、4(2):101-108。 doi:10.1089 / act.1998.4.101
22. S.tarhan、Z.unlu、C.Goktam:変形性膝関節症の患者の磁気共鳴映像法および超音波評価:比較研究。 ClinRheumatology 2003 22:181-18